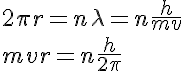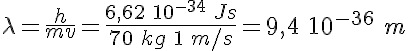3.1 Hipótesis de De Broglie
En 1923, De Broglie lanzó la hipótesis de que la materia en general también presenta el doble comportamiento que presentaba la luz, esa dualidad onda-corpúsculo. No se quedó en el planteamiento cualitativo, extraordinariamente atrevido, sino que lo reflejó en la
expresión  en la que m es
la masa de la partícula,
en la que m es
la masa de la partícula,  la velocidad con la que se mueve y
la velocidad con la que se mueve y 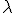 la longitud de onda
asociada a su movimiento.Esta hipótesis fue
comprobada experimentalmente por Davidson y Germer en 1927, que observaron que una corriente de electrones se difractaba,
fenómeno típicamente ondulatorio.
la longitud de onda
asociada a su movimiento.Esta hipótesis fue
comprobada experimentalmente por Davidson y Germer en 1927, que observaron que una corriente de electrones se difractaba,
fenómeno típicamente ondulatorio.
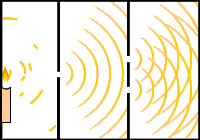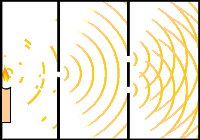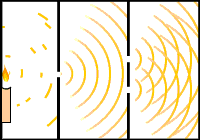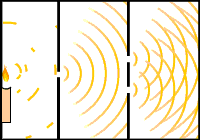
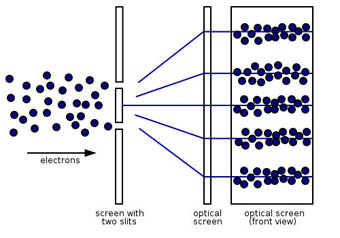
Fíjate en las imágenes. A la izquierda se ve la experiencia de las dos rendijas de Young con una fuente de luz, de manera que interfieren los dos haces de luz. A la derecha se observa el comportamiento ondulatorio de una corriente de electrones que pasa a través de dos rendijas, dando lugar a bandas de interferencia en la pantalla en la que inciden los electrones.
 |
 |
En el caso de un
electrón que se mueva a una velocidad que sea la décima parte de la de la luz,
su onda asociada tiene una 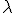 de 0,242 angstroms,
del orden del tamaño de la zona en la que se mueve el electrón del átomo de hidrógeno. Solamente tienes que sustituir en la expresión de De Broglie los valores de la masa del electrón (9,1 10-31 kg), la constante de Planck (6,62 10-34 J.s) y la velocidad de la luz (3 108 m/s).
de 0,242 angstroms,
del orden del tamaño de la zona en la que se mueve el electrón del átomo de hidrógeno. Solamente tienes que sustituir en la expresión de De Broglie los valores de la masa del electrón (9,1 10-31 kg), la constante de Planck (6,62 10-34 J.s) y la velocidad de la luz (3 108 m/s).
 |