8. Equilibrio, medio ambiente y salud
La formación de NO en los motores
 |
La formación de monóxido de nitrógeno a partir de sus elementos tiene lugar según la reacción
N2(g) + O2(g) ↔ 2 NO(g); ΔHº= 180,8 kJ
A temperatura ordinaria, el equilibrio está desplazado casi totalmente a la izquierda, ya que Kc=10-15. Pero al elevar la temperatura hasta los 2000 ºC que se alcanzan en los motores de los automóviles, el equilibrio se desplaza a la derecha, al llegar Kc a valer 0,05. El NO formado contribuye a la formación de lluvia ácida, tras oxidarse y combinarse con el agua.
Para atajar el problema, se utilizan los convertidores catalíticos colocados en los tubos de escape. Como un catalizador es incapaz de desplazar un equilibrio en un sentido o en otro, lo que hace es catalizar la transformación de NO en N2 por reacción con otro contaminante que también se forma en los motores, el CO, en una reacción en la que ambos desaparecen, transformándose en productos inertes:
NO(g) + CO(g) ↔ N2(g) + CO2(g)
La peste del estaño
En algunos órganos de iglesias medievales europeas situados en países con temperaturas muy bajas, se observó que se formaba un polvo gris y que se destruían los tubos de estaño. Dice la leyenda que durante la campaña que Napoleón hizo en Rusia en 1812 los botones de los uniformes se descompusieron, provocando la exposición de sus soldados al intenso frío del invierno ruso.
¿Qué relación tiene la llamada peste del estaño con el equilibrio químico? Se explica porque el estaño tiene dos formas alotrópicas, el estaño blanco y el gris, que están en equilibrio
Sn (gris) ↔ Sn (blanco)
Por debajo de 13 ºC es estable el Sn gris y por encima el blanco, es decir, el proceso anterior es endotérmico.
El Sn gris es frágil y de menor densidad, por lo que en la transformación de estaño blanco a gris hay un importante aumento del volumen, de alrededor del 25%, lo que hace que el metal se rompa.
Como sucede siempre, la velocidad de transformación de una forma en otra disminuye cuando desciende la temperatura. Sin embargo, una pequeña cantidad de polvo de estaño gris sobre la superficie del estaño blanco hace que la transformación hacia el estaño gris se acelere, y eso es lo que sucedía tanto en los tubos de los órganos como en los botones.
Las latas de conserva son envases metálicos, habitualmente de hojalata, que es una fina lámina de acero recubierta por una película de estaño que la protege de la oxidación. ¿Te imaginas qué le podría suceder a una lata de atún que se queda abierta en el frigorífico?
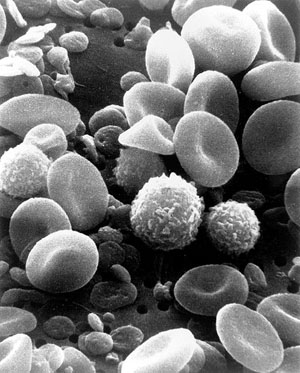
La función de la hemoglobina
 |
En todo momento nuestro cuerpo está consumiendo oxígeno a razón de unos 240 mL por minuto de actividad normal (medidos en condiciones normales). Las distintas partes del organismo necesitan el oxigeno para producir energía por reacción con los hidratos de carbono.
Es la sangre la que se encarga de transportarlo de los pulmones a las células, pero no por simple disolución, ya que de este modo la cantidad sería muy pequeña porque el oxígeno es muy poco soluble en agua. Si se reemplazaran los aproximadamente 5 L de sangre de nuestro cuerpo por agua, ésta sólo podría transportar 15 mL por minuto, frente a los 1000 mL que es capaz de llevar la sangre en las mismas circunstancias, cantidades muy superiores a las del consumo habitual.
La sangre contiene glóbulos rojos, y en cada uno de ellos hay varios cientos de millones de moléculas de hemoglobina, que son las encargadas del transporte del oxígeno. La hemoglobina (Hb para abreviar) tiene una estructura proteínica compleja, que contiene algunos iones Fe2+. Se une con el oxígeno siguiendo una reacción reversible
Hb(aq) + O2(g) ↔ HbO2(aq) en la que se forma oxihemoglobina (HbO2). En los pulmones, donde la concentración de O2 es elevada, la reacción se desplaza casi totalmente a la derecha, formándose oxihemoglobina.
La sangre prosigue su circulación, y a través de arterias y capilares llega a los tejidos. Allí, donde la concentración de O2 es pequeña, se produce un desplazamiento del equilibrio hacia la izquierda. La sangre pierde alrededor de un 45% del O2 que transporta, que es recogido y almacenado por las células.
A continuación lleva hasta los pulmones el CO2 producido en los procesos de oxidación de la célula. La hemoglobina puede unirse también unirse con iones H+, con lo que teniendo en cuenta el equilibrio que existe en la sangre CO2(aq) + H2O(l) ↔ HCO3-(aq) + H+(aq) permite disolver más CO2, facilitando su separación de los tejidos (la sangre transporta el CO2 de tres formas: un 6% disuelto en el plasma, un 24% unido a la hemoglobina y un 70% en forma de HCO3-).
Para que te hagas una idea, el aire inhalado contiene un 20% de O2 y un 0,04% de CO2, y el exhalado un 16% de O2 y un 4% de CO2.
La muerte dulce
Desgraciadamente, además de con el oxígeno, la hemoglobina también se combina con otras moléculas pequeñas y parecidas a la de oxígeno, tales como el monóxido de carbono y el óxido nítrico, si están presentes en los pulmones.
El monóxido de carbono es tóxico porque impide el transporte de oxígeno, ya que se combina con la hemoglobina unas 200 veces más fuertemente que el oxígeno, según el equilibrio
En otras palabras, si están presentes simultáneamente el oxígeno y el monóxido de carbono la hemoglobina se combina preferentemente con el monóxido de carbono, ya que la constante de equilibrio es mayor en el segundo caso que en el primero. En tal situación el aporte de oxígeno se reduce y las células de los tejidos se ven privadas de oxígeno. La muerte proviene a menos que se administre oxígeno puro para romper el equilibrio desplazando las moléculas de monóxido de carbono y cubriendo la deficiencia de oxígeno.
 |
El entrenamiento en altura
Seguro que has oído que un cambio repentino de altitud produce transtornos fisiológicos. La razón reside en que la sustancia que transporta el oxígeno en la sangre es la oxihemoglobina que se produce al combinarse el oxígeno con la hemoglobina, proceso que puede representarse de forma simplifica por el equilibrio:
Hb(aq) + O2(g) ↔ HbO2(aq)
Cuando una persona se traslada a una zona de mayor altitud, la presión parcial del oxígeno en la atmósfera disminuye (a nivel del mar la presión parcial del O2 es de 0,20 atm y en la cima de una montaña de 3000 m es tan sólo de 0,14 atm).
Al producirse una disminución de la presión de oxígeno, también se produce un desplazamiento del equilibrio anterior hacia la formación de Hb, causando la hipoxia (deficiencia de la cantidad de oxígeno que llega a los tejidos del organismo). Si se le da el tiempo suficiente, el organismo puede compensar el efecto produciendo más moléculas de hemoglobina, desplazando el equilibrio de forma gradual hacia la formación de oxihemoglobina. Este aumento se lleva a cabo lentamente y necesita varios días de adaptación.
Si a continuación se traslada a un lugar de menor altitud, el equilibrio se desplazará ahora hacia la formación de mayor cantidad de oxihemoglobina, con lo que aumentará la actividad celular y la resistencia al esfuerzo. Éste es el fundamento del entrenamiento en altura de deportistas que hacen esfuerzos muy largos, como los ciclistas por ejemplo.