5. Energía térmica y temperatura
¿Frío o caliente?
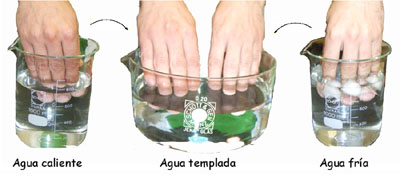
Cuando tocas un objeto puedes identificarlo como caliente o como frío dependiendo de la sensación que te produce. ¿Es precisa esa sensación? El sentido del tacto no permite determinar lo caliente o frío que está un objeto. El tacto proporciona, por tanto, una sensación relativa, ya que depende de lo caliente que se encuentre el objeto que acabas de tocar. Esto lleva a la necesidad de definir una magnitud que permita medir esa sensación: la temperatura.
 |
Movimiento de las partículas, energía térmica y temperatura
Ya sabes que las partículas que forman la materia no están en reposo aunque el cuerpo que constituyan esté quieto. Las partículas de los sólidos vibran continuamente alrededor de su posición de equilibrio, mientras que en los líquidos se mueven unas cerca de otras, ocupando un determinado volumen dentro del recipiente que los contiene; y en los gases se mueven con total independencia unas de otras, ocupando todo el espacio disponible.
También has visto la energía cinética y la energía potencial, y sabes calcularlas en los objetos sin más que saber su masa, su posición y su velocidad. Por tanto, las partículas que constituyen la materia también tienen una determinada energía cinética por el hecho de moverse a una velocidad concreta, y la energía que tiene la sustancia por esa razón se llama energía térmica.
|
|
|
|
|
|
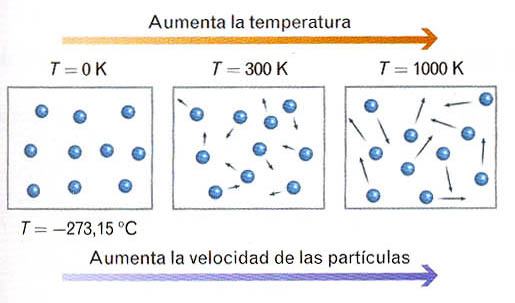
La temperatura de un cuerpo está relacionada con el valor promedio de la energía cinética de dichas partículas, de forma que cuanto mayor sea su energía cinética, mayores serán la energía térmica de la sustancia y su temperatura.
A escala de partículas, las cosas no son tan sencillas. Si tienes una sustancia pura gaseosa a una temperatura dada, no todas las partículas, que son iguales, se mueven a la misma velocidad: hay una distribución de velocidades alrededor de una velocidad promedio, que lleva la mayor parte de las partículas, mientras que unas pocas se mueven a velocidades mayores o menores.
Y si se trata de una mezcla de gases, las partículas de mayor tamaño se mueven más despacio, y las menores más deprisa, de forma que su energía cinética promedio es la misma.
Fíjate en que estás relacionando una propiedad de las partículas (su energía cinética, que depende de la masa y la velocidad de las partículas), que no es observable y no se puede medir directamente, con la temperatura, que es una propiedad macroscópica que puedes medir fácilmente con un termómetro.
La energía cinética que se pierde se transforma en energía térmica, que sirve apara aumentar la temperatura de los cuerpos que por estar en contacto han provocado la pérdida de energía.
Fíjate en la tira cómica siguiente: al dar el tortazo, la mano pierde energía cinética, que se transforma en energía térmica, aumentando la temperatura de la mano y de la cara. Observa que se dice que la energía cinética se transforma en calor, lo que no es conceptualmente correcto, pero es la forma de hablar habitual.

La velocidad de las moléculas
Las moléculas se mueven realmente muy deprisa. Calcula la velocidad con la que se mueve una molécula de hidrógeno (m= 2,02 u) sabiendo que su energía cinética es de 3,735 10-21 J. Ten en cuenta que 1 u equivale a 1,66 10-27 kg.
Temperatura de las sustancias y velocidad de las partículas que las forman
 |