4.1 Teoría electrónica de Lewis
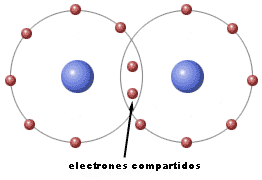
Cuando reaccionan dos átomos que necesitan electrones para adquirir la configuración electrónica de un gas noble y cumplir la regla del octeto, la única posibilidad es que compartan electrones. Las estructuras electrónicas resultantes se llaman estructuras de Lewis y permiten explicar la formación de enlaces covalentes.
Esta teoría electrónica explica también la formación de enlaces covalentes entre elementos metálicos y no metálicos en los que la diferencia de electronegatividad no es muy elevada, con lo que no llegan a formarse iones por transferencia electrónica.
Asimismo, se explican con facilidad sustancias covalentes como el diamante o la sílice.
 |
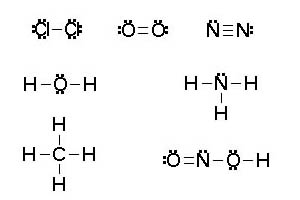 |
- Se determina el número de electrones de la capa más externa de todos los átomos de la sustancia (1 en H, 4 en C, 5 en N, 6 en O, 7 en Cl, etc) y se establece el número total de pares de electrones a distribuir.
- Se colocan los átomos unidos entre sí por un par de electrones. Las distribuciones espaciales de átomos suelen ser simétricas.
- El número de pares resultante se reparte entre todos los átomos de manera que se cumpla la regla del octeto.
- Cada par de electrones se representa por dos puntos o una raya.
-
Si no hay suficiente número de pares de electrones, se utilizan enlaces dobles o triples para alcanzar el octeto.
 |
La regla del octeto no siempre se cumple
La regla del octeto tiene excepciones: hay moléculas en las que el átomo central está rodeado por 2, 3, 5 o 6 pares de electrones, por lo que no se cumple la regla del octeto.
Por ejemplo, el azufre está rodeado por seis pares de electrones en el H2SO4, el nitrógeno por cinco en el ácido nítrico (HNO3), pero el boro solamente por tres pares en el BF3, y el berilio por dos en el BeCl2. ¡Y en todos los casos se trata de moléculas estables!
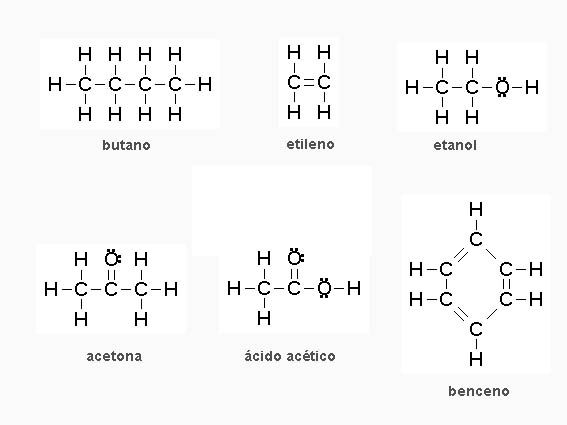
Estructuras de Lewis de compuestos del carbono
Justifica las estructuras de Lewis correspondientes a las moléculas representadas en la imagen anterior.
Enlace covalente coordinado
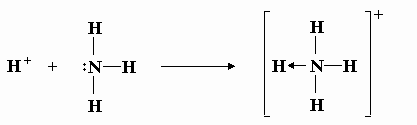
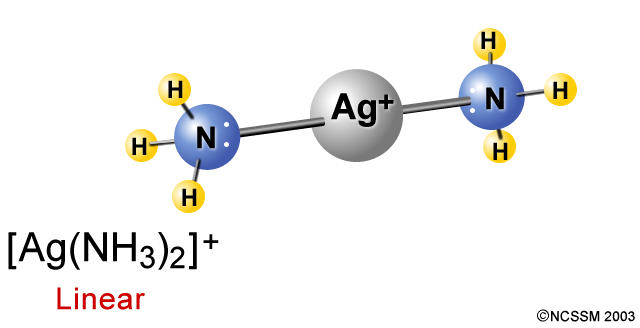
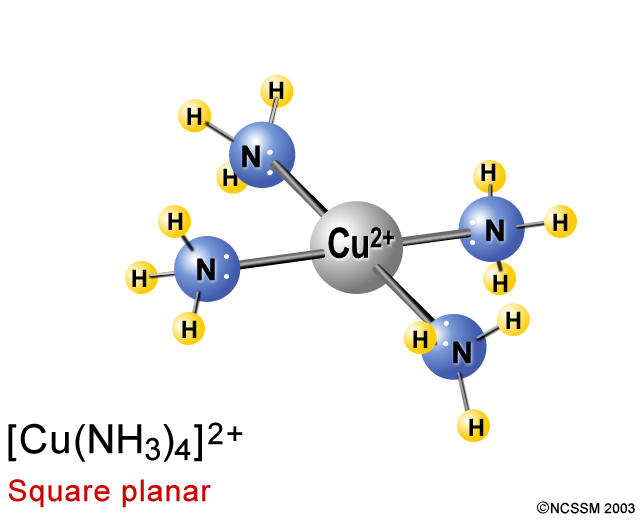
El enlace covalente se forma por compartición de electrones, uno de cada uno de los dos átomos unidos. Pero cuando el par de electrones lo aporta uno de los dos átomos, el enlace se llama covalente coordinado o dativo. Esta circunstancia se da en casos tan importantes como los iones hidronio (H3O+) y amonio (NH4+), así como en los compuestos complejos, como puedes ver en las imágenes.
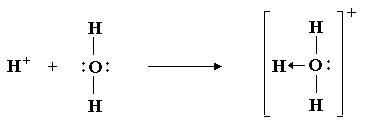 |
 |
 |
 |
Resonancia
Hay moléculas que no se pueden representar por una única estructura de Lewis, sino que hay varias que pueden ser posibles. Ninguna de ellas representa la situación real de la molécula, que se dice que es un híbrido de resonancia de las formas que la representan.
El benceno es uno de los casos más importantes. Tiene seis átomos de carbono y otros seis de hidrógeno. No es que el benceno unas veces tenga una forma y otras veces la otra: el benceno tiene una estructura concreta, pero no se puede representar por una estructura de Lewis única.
Si te fijas, verás que hay tres dobles enlaces alternos en cada forma resonante (estructuras de Kekulé), pero los enlaces entre átomos de carbono son de fuerza intermedia entre el sencillo y el doble. El benceno se suele representar tal y como se muestra en la parte derecha de la imagen.
 |
Uno de los libros tradicionales de Química Orgánica (Allinger-Cava, Ed. Reverté) dice textualmente:
"El rinoceronte proporciona un símil adecuado. El rinoceronte puede considerarse como un híbrido de unicornio y dragón. Lo cual no significa que algunas veces el rinoceronte es un unicornio y otras un dragón, sino que siempre es un rinoceronte.
Todavía más, el rinoceronte es real, mientras que el unicornio y el dragón son imaginarios. Análogamente, el benceno es siempre una estructura única, relacionada con las formas de Kekulé pero diferente de ellas.
Finalmente, el benceno es real, mientras que las formas de Kekulé son imaginarias".