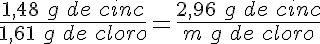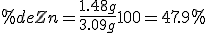1.1 Proporciones constantes
Entre 1794 y 1804, Proust comprobó que cuando dos sustancias se combinan entre sí para formar una tercera, la proporción de combinación en masas entre ellas siempre tiene el mismo valor.
Proporción de combinación y composición centesimal
Utiliza el simulador siguiente con la reacción entre el magnesio y el ácido clorhídrico.
Añade la masa de magnesio que quieras y anota su valor, así como la masa de producto formada una vez terminado el proceso experimental. Este último valor es la suma de la masa de magnesio y la masa de cloro que ha reaccionado. Calcula la relación entre la masa de cloro y la de magnesio. Repite la experiencia con diferentes masas de magnesio y calcula la relación en todos los casos. ¿Cómo es esa relación?
Determina la composicion centesimal del cloruro de magnesio, es decir, el porcentaje de cloro y de magnesio que hay en la sustancia, y también la del cloruro de aluminio, utilizando el mismo procedimiento.
La composición centesimal de las sustancias
Como los elementos se combinan en una proporción constante, la composición de cada sustancia es fija, y el porcentaje en masa que hay en ella de cada elemento (su composición centesimal) también.
Por tanto, si en dos sustancias formadas por los mismos elementos la composición centesimal es diferente, las sustancias son distintas (no tienes más que pensar en los hidrocarburos, de los que se conocen miles, formados todos por carbono e hidrógeno).
Síntesis del cloruro de cinc
Cuando el cinc se hace reaccionar con ácido clorhídrico, se forma cloruro de cinc. Partiendo de 1,48 g de cinc, que reacciona totalmente con exceso de ácido, se obtienen 3,09 g de cloruro de cinc. ¿Qué cantidad de cloro se combinará con 2,96 g de cinc para formar cloruro de cinc? ¿Qué masa se habrá formado de producto?
|
52.1% de cloro y 47.9% de cinc.
| |
|
52.1% de cinc y 47.9% de cloro.
| |
|
65.1% de cloro y 44.9% de cinc
|