1.3 Compuestos ternarios
Los compuestos ternarios son combinaciones
de tres elementos.
Hidróxidos
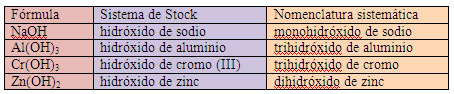
Los hidróxidos están formados por el grupo OH-, que actúa con número de oxidación -1, y un metal.
Para formular, se escribe el
símbolo del metal seguido del OH, entre paréntesis, e intercambia los números
de oxidación como subíndices sin signo. Si el subíndice del grupo OH es 1 no se escribe el paréntesis.
Para nombrar, se utiliza el mismo procedimiento que en los compuestos binarios. Empieza con "hidróxido de", seguido del nombre del metal y utiliza los prefijos numerales o el sistema de Stock.
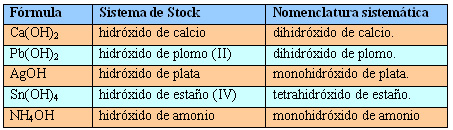
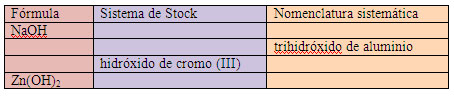
Formulación y nomenclatura (VIII)
Completa la tabla:
Oxoácidos
Son compuestos ternarios formados por hidrógeno, oxígeno y un no metal.
En la tabla siguiente tienes las fórmulas y los nombres de los ácidos oxoácidos, para los que está aceptada la nomenclatura tradicional. Junto a cada uno aparece la fórmula y nombre del ión que forman, y que da lugar a las sales correspondientes (ácido carbónico, ión carbonato).
Lo más práctico es aprender la lista de ácidos e iones.
| H2CO3 (carbónico) CO32- (carbonato) |
|
|
|
| HNO3 (nítrico) NO3- (nitrato) |
HNO2 (nitroso) NO2- (nitrito) |
|
|
| H2SO4 (sulfúrico) SO42- (sulfato) |
H2SO3 (sulfuroso) SO32- (sulfito) |
H2SO2 (hiposulfuroso) SO22- (hiposulfito) |
|
| HClO4 (perclórico) ClO4- (perclorato) |
HClO3 (clórico) ClO3- (clorato) |
HClO2 (cloroso) ClO2- (clorito) |
HClO (hipocloroso) ClO- (hipoclorito) |
La nomenclatura IUPAC resulta más compleja y se utiliza muy poco en este tipo de sustancias: nadie habla del tetraoxosulfato (VI) de hidrógeno, sino del ácido sulfúrico.
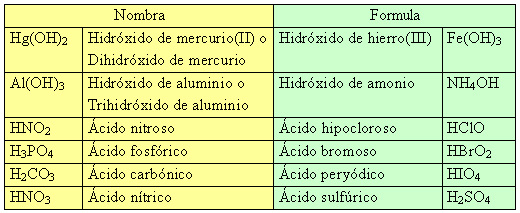
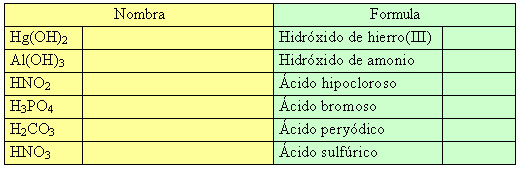
Formulación y nomenclatura (IX)
Formula o nombra:
Oxoaniones
Los oxoaniones son los aniones poliatómicos que resultan de quitar los hidrógenos a los oxoácidos.
Para formular, se escribe la fórmula del oxoácido, se quitan los hidrógenos y se pone, como carga del ión, el número de hidrógenos con signo negativo.
Por ejemplo, en H2SO4, al quitar los dos hidrógenos resulta SO42- y en HNO2, al quitar el hidrógeno resulta NO2-.
Para nombrar, al nombre del oxoácido se le sustituye la palabra "ácido" por "ión" y la terminación -ico por -ato y -oso por -ito. Así, el H2SO4, ácido sulfúrico forma SO42- ión sulfato, y el HNO2, ácido nitroso NO2- forma ión nitrito.
Nomenclatura IUPAC de los oxoaniones
En la nomenclatura IUPAC y de acuerdo con las normas más recientes, los oxoaniones pueden nombrarse de acuerdo con su composición, como sigue:
Prefijo numeral palabra "oxido" nombre del elemento terminado en -ato y, entre paréntesis, la carga del ión. Por ejemplo:
SO42- Tetraoxidosulfato(2-) ; SO32- Trioxidosulfato(2-) ; NO2- Dioxidonitrato(1-)
CO32- Trioxidocarbonato(2-) ; Cr2O72-
Heptaoxidodicromato(2-)
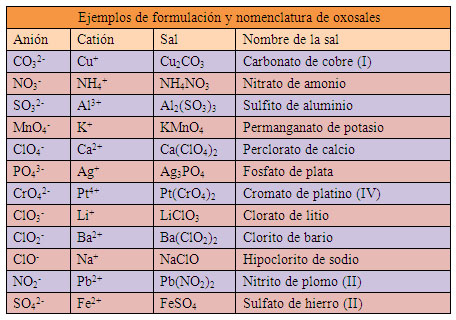
Oxosales
Las oxosales se consideran como un compuesto binario formado por un anión poliatómico (oxoanión) y un catión.
Para formular se escribe el catión seguido del
anión e intercambia las cargas de los iones como subíndices sin signo. Así se consigue que la sal sea neutra, teniendo en cuenta la carga de los iones presentes en el compuesto.
Para nombrar, se nombra el anión sin la carga seguido de la partícula "de" y el nombre del catión.
Las sales que mantienen algún hidrógeno del ácido (sea hidrácido u oxoácido) reciben el mismo nombre pero indicando el número de hidrógenos que tiene. Por ejemplo, el NaHCO3, cuyo nombre vulgar es bicarbonato de sodio se llama también hidrogenocarbonato de sodio.
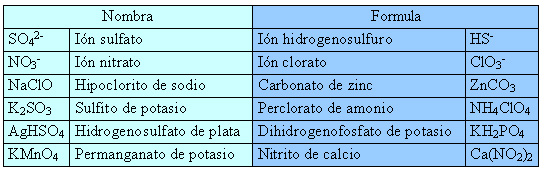
Formulación y nomenclatura (X)
Formula o nombra: