2. Tipos de reacciones químicas

|
Las sustancias reaccionan entre sí de maneras muy diversas: el gran número de reacciones químicas que se producen justifica la necesidad de clasificarlas para su estudio.
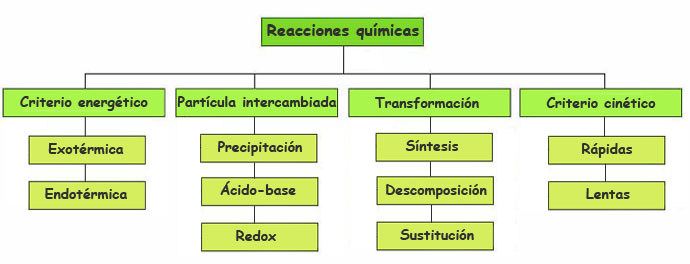
Hay diferentes tipos de reacciones químicas y varias formas de clasificarlas según el criterio elegido. Los criterios que se siguen son generalmente cuatro: el energético, el cinético, la transformación que se produce y la partícula intercambiada.
Criterio energético
- Exotérmicas.
- Endotérmicas.
Criterio cinético
- Rápidas.
- Lentas.
Según la transformación que se produce
- Síntesis.
- Descomposición.
- Sustitución.
Según la partícula intercambiada
- Reacciones ácido-base.
- Reacciones de oxidación-reducción (redox).
- Reacciones de precipitación.
Los aspectos energético y cinético de las reacciones comenzaste a verlos en la Física y química de 4º de ESO, y se desarrollan en la Química de 2º de Bachillerato.
|
|
Ahora vas a trabajar con reacciones clasificadas según la transformación que se produce (cómo se reagrupan los átomos) y según sea la partícula intercambiada (en este caso, también se desarrollan en profundidad en la Química de 2º de Bachillerato, pero hay algunos aspectos que conviene ver ahora por su interés para la Biología y la Geología).
Observa la reacción entre dos gases, amoniaco (NH3) y ácido clorhídrico (HCl), para formar una sal blanca, cloruro de amonio (NH4Cl). Los gases difunden uno hacia otro por el tubo, y en la zona en que entran en contacto se produce la reacción y se forma la sustancia blanca.