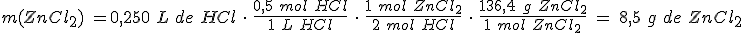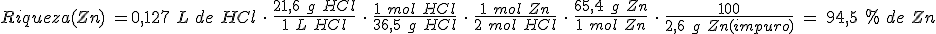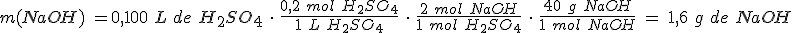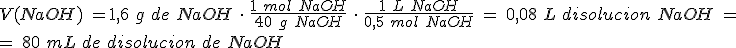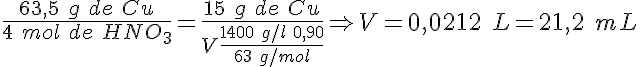3.5 Reactivos en disolución
Hay muchas reacciones químicas que se producen en disolución acuosa. En este caso, los datos o las incógnitas se expresan en forma de volúmenes de disolución. La secuencia de operaciones incluirá un factor que tenga en cuenta la relación entre el volumen de disolución y la cantidad de sustancia de soluto.
Concentración y estequiometría
La forma de expresar la
composición de una disolución permite calcular la cantidad de sustancia del
compuesto disuelto, presente en un volumen de disolución determinado.
La forma habitual de expresar la composición de la disolución es la concentración (c = n/V). Por tanto, el factor de conversión es n = c V.
 |
Disolviendo Zn
En un vaso de precipitados tienes 4,1 g de cinc y les añades 250 mL de una disolución de ácido clorhídrico de concentración 0,5 mol/L. ¿Qué masa de cloruro de cinc se formará? En la reacción se produce también hidrógeno.
 |
Pureza de una muestra de Zn
Para disolver 2,6 g de cinc impuro se han gastado 127 mL de una disolución de HCl de concentración en masa 21,9 g/L. ¿Cuál es la riqueza (pureza) del cinc? (Se supone que las impurezas no reaccionan con el HCl(aq)).
 |
Neutralizando ácido sulfúrico
Dispones de 100 cm3 de disolución de ácido sulfúrico de concentración 0,2 mol/L. ¿Qué masa de NaOH necesitarás para neutralizarlo?
Si el hidróxido de sodio lo tienes en una disolución de concentración 0,5 mol/L, ¿qué volumen de la misma habrá sido necesario para la neutralización anterior?
 |
En la obtención de NO2
El ácido nítrico reacciona con el cobre para formar nitrato de cobre(II), dióxido de nitrógeno (gas rojizo) y agua.
Haces reaccionar una muestra de 15 g de cobre con una disolución de ácido nítrico al 90 % en masa y 1,400 g/mL de densidad. ¿Qué volumen de disolución habrás utilizado, si el cobre ha reaccionado totalmente?