3. La Tabla Periódica
 |
Actualmente se conocen más de 100 elementos químicos. Parece ser que el último, de número atómico 117, lo descubrieron en abril de 2010 dos equipos de investigadores rusos y norteamericanos.
Todos los elementos conocidos están ordenados por filas (periodos) y columnas (grupos) en una tabla bidimensional conocida como Tabla Periódica, de forma que los elementos del mismo grupo tienen propiedades parecidas.
La tabla periódica más famosa es la de Mendeleiev, que este químico ruso publicó en 1869. Como había huecos en la tabla que elaboró, predijo las propiedades de los elementos que deberían estar allí. Unos años después se descubrieron el galio y el germanio, con las propiedades previstas por Mendeleiev.
En la imagen tienes un sello emitido en la URSS (antigua Rusia) en 1969 para conmemorar el centenario de la publicación de la tabla.
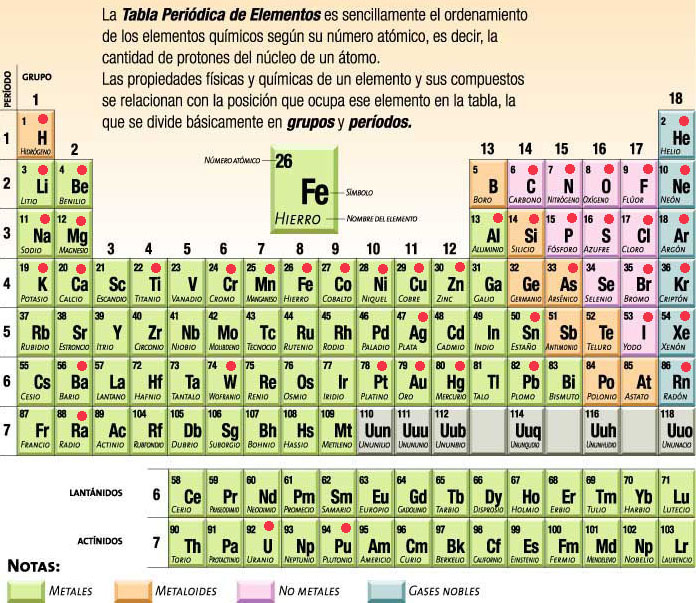
Sin embargo, hoy se utiliza la tabla de Werner y Paneth, publicada ya en el siglo XX (1954). Consta de 18 columnas y 7 filas, además de dos filas fuera de la tabla, como puedes ver en la imagen.
Puedes observar que los elementos se ordenan por orden creciente de número atómico. Es decir, el elemento número 11, que es el sodio, tiene 11 protones y 11 electrones. El elemento siguiente, situado a su derecha, es el 12, el siguiente más a la derecha el 13, y así sucesivamente.
|
¿Qué debes saber de la tabla?
En primer lugar, el nombre y símbolo de los elementos que están marcados con el punto rojo. Además, también tienes que saber el nombre de los siguientes grupos: 1- Alcalinos; 2- Alcalinotérreos; 17- Halógenos; 18- Gases nobles.
Elementos como los alcalinos y los alcalinotérreos son metales, y se caracterizan porque tienen tendencia a perder los pocos electrones que tienen en la capa más externa, de manera que quede completa. Por tanto, se quedan con carga positva, formando cationes. Es lo que le sucede al Na o al Mg, que forman Na+ y Mg2+. Los metales están situados hacia la izquierda de la tabla.
Por otro lado, elementos como el O o el Cl tiene tendencia a ganar electrones, formando aniones, ya que les faltan muy pocos para tener la última capa completa. Son no metales y están situados hacia la derecha de la tabla.
Por último, los gases nobles son los elementos que tienen la última capa completa. Por esa razón no necesitan ganar ni perder electrones.
La regla del octete
En general, los átomos se ionizan ganando o perdiendo electrones para tener completa la última capa electrónica, de forma que los electrones que pierde un átomo para formar un catión los gana otro dando lugar a un anión.
El nombre de los elementos
Realiza la actividad siguiente, asociando el símbolo al nombre de cada elemento, que aparece junto al nombre de origen latino.
La tabla periódica y las estructuras electrónicas
¿Recuerdas el número de electrones que se pueden colocar en cada capa y en las órbitas de cada una de ellas? Pues justamente ese número queda reproducido en la tabla periódica: 2 elementos en el primer periodo, 8 en el segundo y en el tercero (2 + 6), 18 en el cuarto y el quinto (2 + 10 + 6) y 32 en el sexto y el séptimo (2 + 10 + 6 + 14 fuera de la tabla).
Es decir, la forma de la Tabla Periódica está totalmente relacionada con las estructuras electrónicas de los átomos.
Sobre los elementos
Indica si las afirmaciones siguientes son ciertas o falsas:
Verdadero Falso
Verdadero Falso
Verdadero Falso
Verdadero Falso